DNA
Weetjes, Genen, Vragen en Nieuws
Koffie
Er is een enzym dat voor 95% verantwoordelijk is voor de afbraak van cafeïne. Komt uit onze test dat u een langzame variant heeft van dit enzym dan weet u nu beter waarom u nog zo lang wakker ligt na een kop koffie.
Cholesterolverlagers
Bij lagere activiteit van bepaalde enzymen kunnen statines (simvastatine, ...) te langzaam uit het lichaam verwijderd worden. Dan stapelt het medicijn zich op en dat kan stevige bijwerkingen verklaren. Neem de resultaten dus mee naar uw arts.
Operaties
Bij mensen met inactieve varianten van het BCHE gen kunnen spierverslappers, die in noodsituaties (operaties) gebruikt worden, te lang aanhouden waardoor zelfstandig ademen pas later mogelijk is. Een dosisaanpassing lost dit op.
Bloedstolling
Met deze test wordt bepaald hoe uw bloedstolling wordt aangestuurd. Misschien duurt wondheling bij u wel ietsje langer? Dan heeft u op latere leeftijd misschien ook minder snel ontstolling nodig bij preventie van bloedpropjes?
Welke genen worden precies getest?
Onze farmacogenetische test controleert de volgende genen: ABCB1, ALDH2, BCHE, COMT, CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2D6-enhancer, CYP2E1, CYP3A4, CYP3A5, CYP4F2, DPYD, F2, F5, G6PD, GRIK4, HLA-B*1502, IFNL3, MTHFR, OPRM1, SLCO1B1, TPMT, UGT1A1 en VKORC1.
 ABCB1
ABCB1
Een gen dat zorgt voor een transporteiwit. Het vervoert o.a. medicijnen uit bijvoorbeeld de hersenen en de nieren.
 ALDH2
ALDH2
Het ALDH2-gen codeert voor ALDH2, dat staat voor Aldehyde Dehydrogenase 2, een belangrijk enzym dat betrokken is bij alcoholmetabolisme. Aldehyde Dehydrogenase 2 is verantwoordelijk voor de afbraak van een giftige stof, namelijk acetaldehyde.
 BCHE
BCHE
Een gen dat zorgt voor de aanmaak van een enzym dat helpt het lichaam te beschermen tegen bepaalde toxische stoffen door ze af te breken voordat ze de zenuwen bereiken.
 COMT
COMT
COMT is betrokken bij de omzetting van bepaalde “stress” hormonen zoals dopamine en adrenaline, maar ook bijvoorbeeld bepaalde vrouwelijke hormonen.
 CYP1A2
CYP1A2
CYP1A2 is een onderdeel van een grote familie, de cytochroom-P450-enzymen. Ze bevinden zich voornamelijk in de lever. Deze groep is betrokken bij het metabolisme van ongeveer 60% van de medicijnen. 8 tot 10% hiervan wordt door dit gen, CYP1A2, omgezet.
 CYP2B6
CYP2B6
CYP2B6 is een onderdeel van een grote familie, de cytochroom-P450-enzymen. Deze groep is betrokken bij het metabolisme van ongeveer 60% van de medicijnen. Ongeveer 4% van de 200 meest voorgeschreven en gebruikte medicijnen, waaronder voornamelijk antivirale middelen, worden afgebroken door CYP2B6.
 CYP2C8
CYP2C8
CYP2C8 is een onderdeel van een grote familie, de cytochroom-P450-enzymen. Deze groep is betrokken bij het metabolisme van ongeveer 60% van de medicijnen. Dit enzym is goed voor 7% van het totale CYP-enzymgehalte in de lever.
 CYP2C9
CYP2C9
CYP2C9 is een onderdeel van een grote familie, de cytochroom-P450-enzymen. Deze groep is betrokken bij het metabolisme van ongeveer 60% van de medicijnen. Ongeveer 10%-20% van alle medicijnen worden (deels) door CYP2C9 omgezet.
 CYP2C19
CYP2C19
CYP2C19 is een onderdeel van een grote familie, de cytochroom-P450-enzymen. Deze groep is betrokken bij het metabolisme van ongeveer 60% van de medicijnen. Ongeveer 8% van alle medicijnen worden (deels) door CYP2C19 omgezet, waaronder bijvoorbeeld antidepressiva, maagmiddelen (de protonpompremmers) en antistollingsmiddelen.
 CYP2D6
CYP2D6
CYP2D6 is onderdeel van de cytochroom-P450-enzymen, dit zijn enzymen die voornamelijk in de lever werken en zorgen voor de afbraak van zeer veel diverse stoffen in het lichaam. Dit gen is betrokken bij zeker 25% van de door artsen voorgeschreven medicijnen, zoals antidepressiva, antipsychotica, opioiden, tamoxifen, anti-aritmica.
 CYP2E1
CYP2E1
CYP2E1 is onderdeel van de cytochroom-P450-enzymen, dit zijn enzymen die voornamelijk in de lever en in minder mate in de hersenen, longen en nieren werken. Ze zorgen voor de afbraak van zeer veel diverse stoffen in het lichaam.
 CYP3A4
CYP3A4
CYP3A4 is onderdeel van de cytochroom-P450-enzymen. Dit enzym is een van de belangrijkste CYP-enzymen omdat het verantwoordelijk is voor de verwerkingvan ongeveer 45-60% van de voorgeschreven medicijnen.
 CYP3A5
CYP3A5
CYP3A5 is onderdeel van de cytochroom-P450-enzymen, dit zijn enzymen die voornamelijk in de lever en in minder mate in de hersenen, longen en nieren werken. Ze zorgen voor de afbraak van zeer veel diverse stoffen in het lichaam.
 CYP4F2
CYP4F2
CYP4F2 reguleert de biologische beschikbaarheid van vitamine E en vitamine K. Variaties in CYP4F2 die de biologische beschikbaarheid van vitamine K beïnvloeden, hebben ook invloed op de dosering van vitamine k-antagonisten zoals warfarine of acenocoumarol.
 DPYD
DPYD
Dit gen speelt een centrale rol. Het is namelijk betrokken bij de afbraak van de moleculen uracil en thymine. Dit zijn bouwstenen van het DNA en het aanverwante-RNA.
 F2
F2
Het F2-gen bevat instructies voor het maken van een eiwit dat protrombine wordt genoemd. Dit is een stollingsfactor die belangrijk is bij de bloedstolling.
 F5
F5
Het F5-gen bevat instructies voor het maken van een eiwit dat coagulatiefactor V (5) wordt genoemd. Dit is een stollingsfactor die belangrijk is bij de bloedstolling.
 G6PD
G6PD
Het G6PD-gen geeft instructies voor het maken van een enzym genaamd glucose-6-fosfaatdehydrogenase. Dit enzym speelt een cruciale rol in rode bloedcellen. Variaties in dit gen leiden tot G6PD-deficientie wat zich manifesteert als een acute hemolytische anemie.
 GRIK4
GRIK4
GRIK4 codeert voor een eiwit wat signalen van de neurotransmitter glutamaat doorgeeft in de hersenen. Er is nog niet veel met zekerheid te zeggen over dit gen, maar variaties in dit gen worden in verband gebracht met hoe je lichaam reageert op anti-depressiva.
 HLA-B
HLA-B
HLA-B is een belangrijk onderdeel van het immuunsysteem. Het hoort bij een familie van genen, het HLA-complex. Het helpt het immuunsysteem onderscheid te maken tussen je eigen eiwitten en eiwitten van een binnendringer, zoals een bacterie of een virus.
 IFNL3
IFNL3
IFNL3 is een gen wat codeert voor een cytokine. Cytokines zijn belangrijke signaaleiwitten in het immuunsysteem. Wanneer er een bedreiging wordt gesignaleerd in je lichaam worden er veel cytokines geactiveerd waardoor de afweerreactie op gang kan komen.
 MTHFR
MTHFR
Het MTHFR gen codeert voor het enzym methyleentetrahydrofolaatreductase. Ditenzym is betrokken bij het foliumzuurmetabolisme. Dit foliumzuurmetabolisme isessentieel voor de productie van DNA en de eiwitsynthese die op hun beurt weer essentieel zijn voor alle lichaamsfuncties.
 OPRM1
OPRM1
Het OPRM1-gen bevat instructies voor het maken van een eiwit dat de mu (μ)-receptor wordt genoemd. Dit is een normaal onderdeel van ons lichaam en het is een systeem waar pijn, beloning maar ook verslaving worden gereguleerd.
 SLCO1B1
SLCO1B1
Dit SLCO1B1-gen bevat de instructies voor het maken van een eiwit dat organisch aniontransporterend polypeptide 1B1 of OATP1B1 wordt genoemd. Hetheeft invloed op het vervoer van stoffen in het lichaam. Het eiwit wordt gevondenin levercellen waar het verbindingen uit het bloed naar de lever transporteert, zodat ze uit het lichaam kunnen worden verwijderd.
 TPMT
TPMT
Het TPMT gen codeert voor het enzym thiopurine S-methyltransferase. Net als COMT (ook een methyltrasferase) is TPMT betrokken bij de ontgifting van het lichaam. TPMT wordt voornamelijk gevonden in de lever en de nieren en komt wat minder voor in de hersenen en longen.
 UGT1A1
UGT1A1
Dit gen behoort tot een familie van genen die instructies geven voor het maken van enzymen die UDP-glucuronosyltransferasen worden genoemd. Deze enzymenvoeren een reactie uit, glucuronidering genoemd: dit proces is een handigheidje van het lichaam om verschillende stoffen meer wateroplosbaar te maken en op deze manier makkelijker door het lichaam te vervoeren of uit het lichaam te verwijderen via urine of de ontlasting met behulp van gal (uit de lever).
 VKORC1
VKORC1
Dit gen codeert voor een enzym in de lever dat een sleutelrol heeft in de vitamine K-cyclus. Vitamine K speelt een belangrijke rol bij het helpen maken van een bloedstolsel en dus het voorkomen van overmatig bloeden.
Veelgestelde vragen
Over welke medicijnen hebben we het dan?
 Via onze medicijnpagina’s kunt u achterhalen welke medicijnen beinvloed worden door jouw DNA.
Elk medicijn heeft in een duidelijk kader staan of er een invloed is (zie voorbeeld hiernaast).
Via onze medicijnpagina’s kunt u achterhalen welke medicijnen beinvloed worden door jouw DNA.
Elk medicijn heeft in een duidelijk kader staan of er een invloed is (zie voorbeeld hiernaast).
De aard van de invloed en
welke genen betrokken zijn staan er echter niet vermeld. Die informatie kunt u terugvinden in uw
account onder mijn medicijnen.
Verdere uitleg vindt u in uw rapportage wanneer u een farmacogenetische test heeft uitgevoerd.
Wat kan ik verwachten?
 Na ontvangst van uw bestelling gaan we aan de slag met uw testkit. Uw testkit wordt per post verzonden en past in uw brievenbus.
Na ontvangst van uw bestelling gaan we aan de slag met uw testkit. Uw testkit wordt per post verzonden en past in uw brievenbus.
De afbeelding hiernaast laat zien wat u ontvangt.
Hoe werkt de DNA verzameling?
Het is erg simpel: onze test-kit bevat een speciaal wattenstaafje waarmee je gemakkelijk speeksel kan verzamelen door het langs de binnenkant van je wang te bewegen. Het wattenstaafje stuur je in de retour-envelop aan ons terug en wij zorgen dat het lab er mee aan de slag gaat.
 Hoe kan ik mijn DNA resultaten delen met mijn arts of apotheker?
Hoe kan ik mijn DNA resultaten delen met mijn arts of apotheker?
Het is erg eenvoudig om een behandelaar inzage te geven in de DNA resultaten.
Ga in het menu naar ‘mijn behandelaren’ en klik op de button ‘Voeg een behandelaar toe”. Je doorloopt de vragen en geeft zo aan wat je met wie wilt delen.
Als laatste stap kun je kiezen of de uitnodiging per email verstuurd moet worden of dat je liever een de uitnodiging uitprint en meeneemt naar een afspraak.
 Hoe lang duurt het?
Hoe lang duurt het?
We streven ernaar de resultaten van het lab met 3-5 weken aan je te kunnen aanbieden.
Als het zover is ontvang je van ons een email. Je resultaten staan dan overzichtelijk weergegeven
in jouw account.
 Wordt deze test door de zorgverzekering vergoed?
Wordt deze test door de zorgverzekering vergoed?
Farmacogenetische testen worden vergoed als een patiënt ernstige bijwerkingen heeft of als het medicijn onverwacht ineffectief is. Het heeft dus zeker zin om de factuur bij uw zorgverzekeraar in te dienen.
 Waaruit halen jullie DNA?
Waaruit halen jullie DNA?
We gebruiken alleen maar wat wangslijmvlies. Even schrapen met een wattenstaafje aan de binnenkant van
je wang en je bent klaar.
Dus: geen naalden en geen bloed!
 Van wie zijn de DNA resultaten?
Van wie zijn de DNA resultaten?
Dat is makkelijk: van jou!
Jij bepaalt wat er gebeurt met jouw gegevens. Wij zorgen ervoor dat dat op de meest betrouwbare en
veilige manier gebeurt. Wij kunnen je meer informatie over jouw genen geven als je de gegevens bij
ons laat staan, maar je kan ze ook bij ons verwijderen. Dat is jouw keuze, de gegevens zijn immers
van jou.
 Gebruiken jullie mijn data verder?
Gebruiken jullie mijn data verder?
Nee.
Het zijn jouw gegevens. En mochten we tegen een goed onderzoek aanlopen waar we graag onze medewerking
aan willen verlenen om de wetenschap een stap verder te helpen, dan vragen we dat gewoon aan jou.
Zonder jouw expliciete toestemming, op dat moment, gebeurt er niets.
 Staan mijn gegevens veilig bij jullie?
Staan mijn gegevens veilig bij jullie?
Wij doen onze uiterste best om te voorkomen dat er nare dingen gebeuren: we hebben maatregelen genomen om illegale toegang te voorkomen zodat jouw genetische informatie bij ons veilig is.
- Volledig gescheiden databases houden uw genetische informatie ontkoppeld van uw persoonlijk (identificeerbare) informatie.
- Alle verbindingen met onze website zijn gecodeerd met behulp van TLS/SSL (Transport Layer Security/Secure Sockets Layer) technologie.
- Externe firewalls beperken ongeautoriseerde verbindingen met onze databases.
 Hoe krijg ik mijn uitslag?
Hoe krijg ik mijn uitslag?
Wij sturen je een email zodra de gegevens van het lab bij ons binnen zijn.
Binnen jouw account zijn alle geteste data overzichtelijk weergegeven.
We geven duidelijk aan wat de uitslag betekent en welke impact dat voor jou kan hebben.
 Voeren jullie de test zelf uit?
Voeren jullie de test zelf uit?
Voor de DNA analyse werken we samen met een gevestigd en geaccrediteerd laboratorium. Zo kunnen we een hoge kwaliteit DNA analyse aanbieden.
 Wat zijn de mogelijke uitslagen?
Wat zijn de mogelijke uitslagen?
- PM, poor metabolizer - sterk verminderde of geen activiteit
- IM, intermediate metabolizer - verminderde activiteit
- EM, extensive metabolizer - normale activiteit
- UM, ultrarapid metabolizer - zeer snelle activiteit
 Fran Lowry, 6 juni 2019
Farmacogenetisch testen kan artsen helpen om met grotere precisie het meest effectieve antidepressivum
te kiezen voor hun patiënten met depressieve stoornis (MDD).
Fran Lowry, 6 juni 2019
Farmacogenetisch testen kan artsen helpen om met grotere precisie het meest effectieve antidepressivum
te kiezen voor hun patiënten met depressieve stoornis (MDD).Een onderzoek dat de bruikbaarheid van dergelijke testen onderzocht, toonde aan dat remissie, respons en verlichting van depressieve symptomen groter waren bij patiënten bij wie de zorg werd geleid door dergelijke testen, in vergelijking met patiënten die behandeling zoals gewoonlijk (TAU) kregen, zonder genetische begeleiding.
“Farmacogenetische testen zullen ons van tevoren niet vertellen welk antidepressivum het meest effectief is voor een patiënt, althans niet op dit moment. Maar dergelijke tests helpen ons te weten welke geneesmiddelen mogelijk niet kloppen of niet de beste keuze of onjuist zijn voor een bepaalde patiënt, “zei onderzoeker John F. Greden, MD, uitvoerend directeur, University of Michigan Comprehensive Depression Center, en Rachel Upjohn hoogleraar Psychiatrie, Ann Arbor.
Farmacogenetisch testen wordt nog niet routinematig door artsen toegepast als een manier om de resultaten voor patiënten met MDD te verbeteren.
“Er is veel scepsis over dergelijke tests, er is verwarring, mensen zijn hierover verbaasd, maar daar zijn redenen voor. Een voorbeeld: vroege studies en publicaties over farmacogenetica bestudeerden kleine aantallen genen en varianten en hadden kleine steekproefgroottes en korte duur van de follow-up. Maar dergelijke testen hebben een lange weg afgelegd sinds de vroege dagen, “zei Greden.
“Als artsen weten hoe ze farmacogenetische-gegevens moeten gebruiken, helpt het hen om keuzes te maken die respons en remissie tot stand brengen,” voegde hij eraan toe.
 Jacqueline Howard, 2 juni 2019
Onderzoekers weten al lang dat verschillende soorten kanker, behalve borst- en eierstokken, in verband worden
gebracht met schadelijke mutaties bij BRCA1 en BRCA2, waaronder eileiderkanker, prostaatkanker en
alvleesklierkanker.
Jacqueline Howard, 2 juni 2019
Onderzoekers weten al lang dat verschillende soorten kanker, behalve borst- en eierstokken, in verband worden
gebracht met schadelijke mutaties bij BRCA1 en BRCA2, waaronder eileiderkanker, prostaatkanker en
alvleesklierkanker.Een nieuwe studie, gepresenteerd op de jaarlijkse bijeenkomst van de American Society for Clinical Oncology in Chicago, beschrijft een behandelaanpak specifiek voor patiënten met gemetastaseerde alvleesklierkanker die een BRCA1- of BRCA2-mutatie hadden.
Terwijl ze op zoek waren naar een verklaring van de interindividuele variabiliteit in pijnperceptie en door drugs veroorzaakte pijnverlichting, hebben wetenschappers geprobeerd de antwoorden in de genen te vinden. Vanaf deze publicatie hebben onderzoekers ten minste zes genen of genclusters geïdentificeerd (meestal geassocieerd met opioïde, adrenerge en catecholamine-routes) die mogelijk verband houden met de ontwikkeling van pijn.
Veel artsen hebben al ervaring met het grote voordeel van de implementatie van farmacogenomica in hun dagelijkse praktijk. Doseringsaanpassingen volgens het genotype van een patiënt om de medicamenteuze behandeling te optimaliseren, zijn geïmplementeerd in relevante klinische richtlijnen en in samenvattingen van productkenmerken (SmPC) voor bepaalde geneesmiddelen en medicijnklassen. Dienovereenkomstig wordt het vertalen van genomische gegevens in de klinische praktijk steeds belangrijker in het begrijpen van verschillen in het effect van medicatie tijdens de behandeling van pijn.
 EMA, 15 maart 2019
Het Europese Geneesmiddelenbureau heeft een evaluatieonderzoek gestart van geneesmiddelen die fluorouracil bevatten en de gerelateerde geneesmiddelen capecitabine, tegafur en flucytosine, die in het lichaam worden omgezet in fluorouracil.
De evaluatie zal bestaande screeningsmethoden en hun waarde onderzoeken bij het identificeren van patiënten met een verhoogd risico op ernstige bijwerkingen.
EMA, 15 maart 2019
Het Europese Geneesmiddelenbureau heeft een evaluatieonderzoek gestart van geneesmiddelen die fluorouracil bevatten en de gerelateerde geneesmiddelen capecitabine, tegafur en flucytosine, die in het lichaam worden omgezet in fluorouracil.
De evaluatie zal bestaande screeningsmethoden en hun waarde onderzoeken bij het identificeren van patiënten met een verhoogd risico op ernstige bijwerkingen.
 Sonya Collins, 28 februari 2019
Deze maand vierde Karen Daggett 10 jaar van het leven waarvan ze dacht dat ze het niet zou hebben.
Op Valentijnsdag 2009 voelde ze zich niet goed genoeg om samen met haar vrienden op het eiland Marco
Island in Florida een koppel te dineren. Maar haar man stond erop dat ze met hem meeging, en daarvoor is
Daggett dankbaar. “Als ik die avond [alleen] was gebleven, was ik waarschijnlijk gestorven”, zei ze.
Sonya Collins, 28 februari 2019
Deze maand vierde Karen Daggett 10 jaar van het leven waarvan ze dacht dat ze het niet zou hebben.
Op Valentijnsdag 2009 voelde ze zich niet goed genoeg om samen met haar vrienden op het eiland Marco
Island in Florida een koppel te dineren. Maar haar man stond erop dat ze met hem meeging, en daarvoor is
Daggett dankbaar. “Als ik die avond [alleen] was gebleven, was ik waarschijnlijk gestorven”, zei ze.Verschillende genen vertellen het lichaam hoe verschillende medicijnen af te breken. Een variant in een van die genen kan van invloed zijn op de manier waarop u één, enkele of alle medicijnen verwerkt waarvoor het gen verantwoordelijk is. Sommige genvarianten kunnen u zo gevoelig maken voor een medicijn dat u slechts de helft minder nodig hebt dan de meeste mensen om hetzelfde effect te krijgen. Een andere variant zou kunnen betekenen dat je twee keer zoveel nodig hebt. Weer een ander kan ertoe leiden dat u mogelijk een fatale reactie krijgt op bepaalde medicijnen.
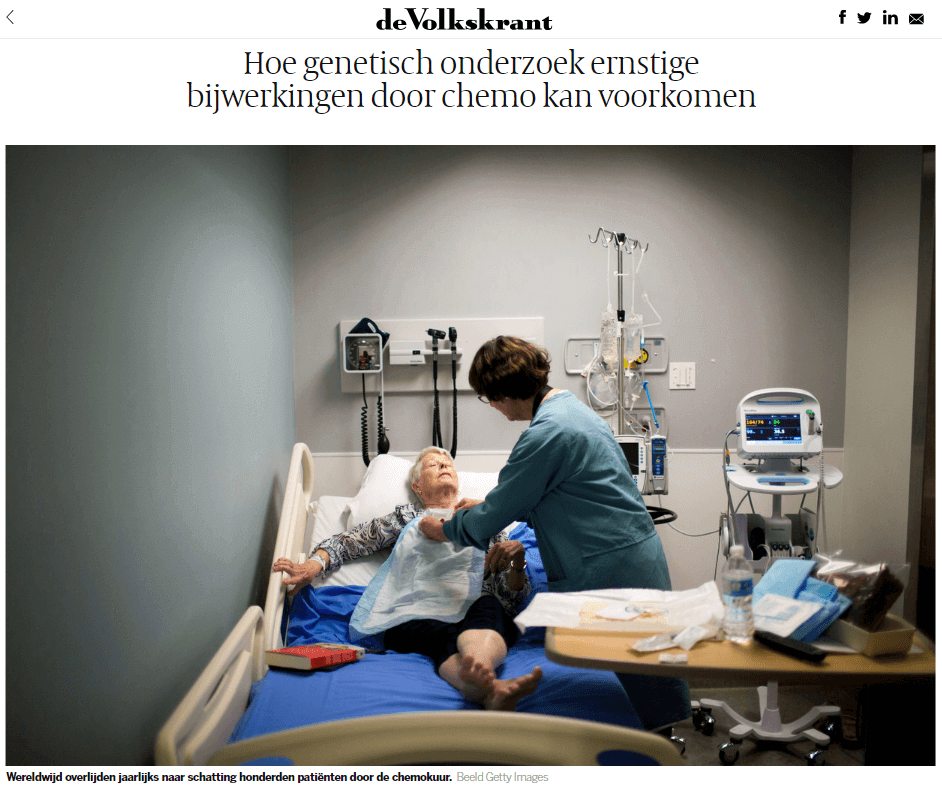 Ellen de Visser, 2 januari 2019
Het aantal kankerpatiënten dat ernstig ziek wordt of zelfs overlijdt door het veelgebruikte chemomedicijn
5-FU kan drastisch omlaag door alle patiënten vooraf genetisch te testen en daarna eventueel de dosis aan
te passen. Nederlands onderzoek onder elfhonderd patiënten in zeventien ziekenhuizen levert daarvoor nu
het definitieve bewijs.
Ellen de Visser, 2 januari 2019
Het aantal kankerpatiënten dat ernstig ziek wordt of zelfs overlijdt door het veelgebruikte chemomedicijn
5-FU kan drastisch omlaag door alle patiënten vooraf genetisch te testen en daarna eventueel de dosis aan
te passen. Nederlands onderzoek onder elfhonderd patiënten in zeventien ziekenhuizen levert daarvoor nu
het definitieve bewijs.De belangrijkste verklaring daarvoor is al jaren bekend. 5-FU, dat via een infuus of per pil wordt toegediend, wordt door een enzym in de lever afgebroken tot een inactieve stof. Maar 8 procent van alle mensen heeft een genetische variatie waardoor dat enzym niet of minder actief is. Gevolg: het medicijn wordt te traag of helemaal niet afgebroken, waardoor het gehalte aan werkzame stof in het bloed hoog blijft en het medicijn de kans krijgt om gezonde weefsels ernstig aan te tasten. In hun dna werd gezocht naar de vier meestvoorkomende variaties die de activiteit van het betrokken enzym verminderen of uitschakelen. Bij de 85 patiënten met een van de onderzochte variaties werd de dosis van het kankermedicijn aangepast, ze kregen een kwart tot de helft minder. Het aantal patiënten met ernstige bijwerkingen halveerde, staat beschreven in The Lancet Oncology.
De mijnmedicijn personal medicine test niet alleen die 4 variaties maar daarnaast ook nog vele anderen waarvan u de resultaten mee kunt nemen naar uw behandelend arts.
Verschillende studies tonen aan dat deze aandoening een belangrijke en complexe genetische component heeft die betrekking heeft op de behandeling met medicijnen. Er zijn veel polymorfismen van genen die betrokken zijn bij het metabolisme van geneesmiddelen geanalyseerd. Deze onderzoeken tonen veel genvariaties aan, met name op CYP450 (die 90% van de geneesmiddelen metaboliseert) en vormen het meest geschikte aanknopingspunt voor zowel de huidige als de toekomstige migraine-therapie. Farmacogenetica beloven te kunnen helpen bij het vinden van een farmacologische therapie op basis van de unieke genetische kenmerken van de patiënt.
 Emily Pond, 7 September 2018
Het gebruik van farmacogenetica bij de behandeling van depressieve stoornissen wordt ondersteund door
onderzoeksgegevens gepubliceerd in het Journal of Psychiatry Research.
Emily Pond, 7 September 2018
Het gebruik van farmacogenetica bij de behandeling van depressieve stoornissen wordt ondersteund door
onderzoeksgegevens gepubliceerd in het Journal of Psychiatry Research.
 Batya Swift Yasgur, 30 mei 2018
Het vinden van een, voor een bepaalde patiënt, effectief en verdraagbaar antidepressivum kan lange tijd
duren. Gedurende deze tijd worden patiënten blootgesteld aan ineffectieve medicatie met potentiële
nadelige effecten en de schadelijke effecten van de depressie zelf.
De redenen voor een negatieve reactie op antidepressiva kunnen complex zijn, maar genetische
componenten zijn duidelijk relevant.
Het gebruik van farmacogenetica bij behandelingen met antidepressiva is daarom bedoeld om de
remissiepercentages van depressie te verbeteren en de nadelige effecten te verminderen.
Batya Swift Yasgur, 30 mei 2018
Het vinden van een, voor een bepaalde patiënt, effectief en verdraagbaar antidepressivum kan lange tijd
duren. Gedurende deze tijd worden patiënten blootgesteld aan ineffectieve medicatie met potentiële
nadelige effecten en de schadelijke effecten van de depressie zelf.
De redenen voor een negatieve reactie op antidepressiva kunnen complex zijn, maar genetische
componenten zijn duidelijk relevant.
Het gebruik van farmacogenetica bij behandelingen met antidepressiva is daarom bedoeld om de
remissiepercentages van depressie te verbeteren en de nadelige effecten te verminderen.
 Robert H. Shmerling, 12 januari 2018
Statines zijn in Nederland veel voorgeschreven medicijnen. Statines zijn de eerste keuze voor artsen.
Robert H. Shmerling, 12 januari 2018
Statines zijn in Nederland veel voorgeschreven medicijnen. Statines zijn de eerste keuze voor artsen.Gemiddeld genomen stopt ongeveer 50% van de patiënten met statine medicijnen. Dit heeft verschillende oorzaken. Er wordt geen verbetering gevoeld en/of er is sprake van bijwerkingen en/of men gelooft publiciteit, waarin de werking in twijfel wordt getrokken. Vaak start zo’n 25% weer opnieuw met een ander statine medicijn. 25% echter kiest ervoor om geen statine medicijn meer te gebruiken, vanwege de vervelende bijwerkingen.
In Chicago is een onderzoek gedaan met patiënten, die gestopt waren met statine medicijnen. Bij hen werd een DNA-test afgenomen en op basis hiervan werd een bij het gevonden DNA-profiel passende statine medicijn voorgeschreven. Bijna 60% van deze groep was weer bereid om met de nieuwe medicatie door te gaan.
Na 8 maanden waren de cholesterol waardes lager. Van de controlegroep, waar de DNA-test niet is afgenomen, was slecht 33% bereid om opnieuw te beginnen met statine medicijnen te gebruiken.
 KNMP, 13 april 2017
Bij 200.000 medicijnrecepten in 2016 zou de dosis aangepast zijn als apothekers het DNA-profiel voor
medicijnafbraak hadden kunnen aanvragen.
KNMP, 13 april 2017
Bij 200.000 medicijnrecepten in 2016 zou de dosis aangepast zijn als apothekers het DNA-profiel voor
medicijnafbraak hadden kunnen aanvragen.
Atherosclerose is wereldwijd een overheersende oorzaak van sterfte en morbiditeit. Statines behoren tot de meest voorgeschreven klassen van geneesmiddelen, en hun voorschrijfindicaties en doelpopulaties zijn aanzienlijk uitgebreid in de officiële richtlijnen die onlangs zijn gepubliceerd door de Amerikaanse en Europese expertpanels. Nadelige effecten van statine farmacotherapie leiden echter tot aanzienlijke kosten en morbiditeit en kunnen leiden tot niet-therapietrouw en stopzetting van de therapie. Met statine geassocieerde spiersymptomen komen voor bij ~ 10% van de patiënten op statines en vormen het meest gemelde bijwerkingeneffect dat geassocieerd is met statine farmacotherapie. Aanzienlijke klinische en niet-klinische onderzoeksinspanningen zijn gericht op het bepalen of genetica een zinvol inzicht kunnen bieden met betrekking tot het risico van statine-nadelige effecten van een individuele patiënt. Deze eigentijdse beoordeling van het relevante klinische onderzoek naar polymorfismen in verschillende sleutelgenen die de farmacokinetiek van statine beïnvloeden (bijv. Transporters en metaboliserende enzymen), statinewerkzaamheid (bijv. Medicijndoelwitten en pathways) en giftigheid van endorganen (bijv. Myopathieroutes) hoogtepunten verschillende veelbelovende farmacogenomische kandidaten. SLCO1B1 521C is momenteel echter de enige klinisch relevante farmacogenetische test met betrekking tot statine-toxiciteit en de relevantie ervan is beperkt tot simvastatine-myopathie.











Volg ons op...