DNA
Invloed van genen op het risico van de ziekte van Alzheimer
Benieuwd naar jouw genetisch risico voor de ziekte van Alzheimer? Heeft iemand in jouw familie last van de ziekte van Alzheimer? Hoewel Alzheimer een complexe aandoening is die wordt beïnvloed door leeftijd, familiegeschiedenis, cardiovasculaire gezondheid en levensstijlkeuzes, spelen genetica toch een cruciale rol als risicofactor.

De ziekte van Alzheimer gaat over complexe mechanismen die de functie en structuur van de hersenen beïnvloeden. Genetische variaties kunnen factoren zoals de vorming van amyloïde plaques, abnormale tau-eiwitten en ontstekingen beïnvloeden, wat kan bijdragen aan de ontwikkeling van de ziekte.
Risico op de ziekte van Alzheimer en Meamedica
Genetische factoren spelen een belangrijke rol bij het bepalen van de individuele gevoeligheid voor de ziekte van Alzheimer. Terwijl andere factoren zoals leeftijd, familiegeschiedenis, cardiovasculaire gezondheid en levensstijlkeuzes zoals dieet en lichaamsbeweging ook cruciale rollen spelen, kunnen genetische variaties in bepaalde genen belangrijke aspecten van de pathologie van Alzheimer beïnvloeden, waaronder:
- Vorming van amyloïde plaques
- Afwijkingen in tau-eiwitten
- Neuro-inflammatie
- Neuronale dood en synaptische disfunctie
Het begrijpen van deze genetische invloeden kan helpen bij het definiëren van proactieve maatregelen zoals het handhaven van een gezonde levensstijl, het beheersen van cardiovasculaire risicofactoren, stimulatie van de mentale activiteit, het onderhouden van sociale contacten en het raadplegen van zorgverleners voor gepersonaliseerde begeleiding en ondersteuning ter vermindering van het mogelijk verhoogde risico op de ziekte van Alzheimer.
Dementie
Alzheimer en dementie, wat zijn de verschillen? In feite is Alzheimer een type dementie.
Dementie is een breed begrip dat wordt gebruikt om een achteruitgang in cognitieve functie te beschrijven die ernstig genoeg is om het dagelijks leven te belemmeren. Het is geen specifieke ziekte, maar eerder een groep symptomen geassocieerd met geheugenverlies, denkvaardigheden en andere mentale vermogens. Dementie is meestal progressief, wat betekent dat het in de loop van de tijd erger wordt.
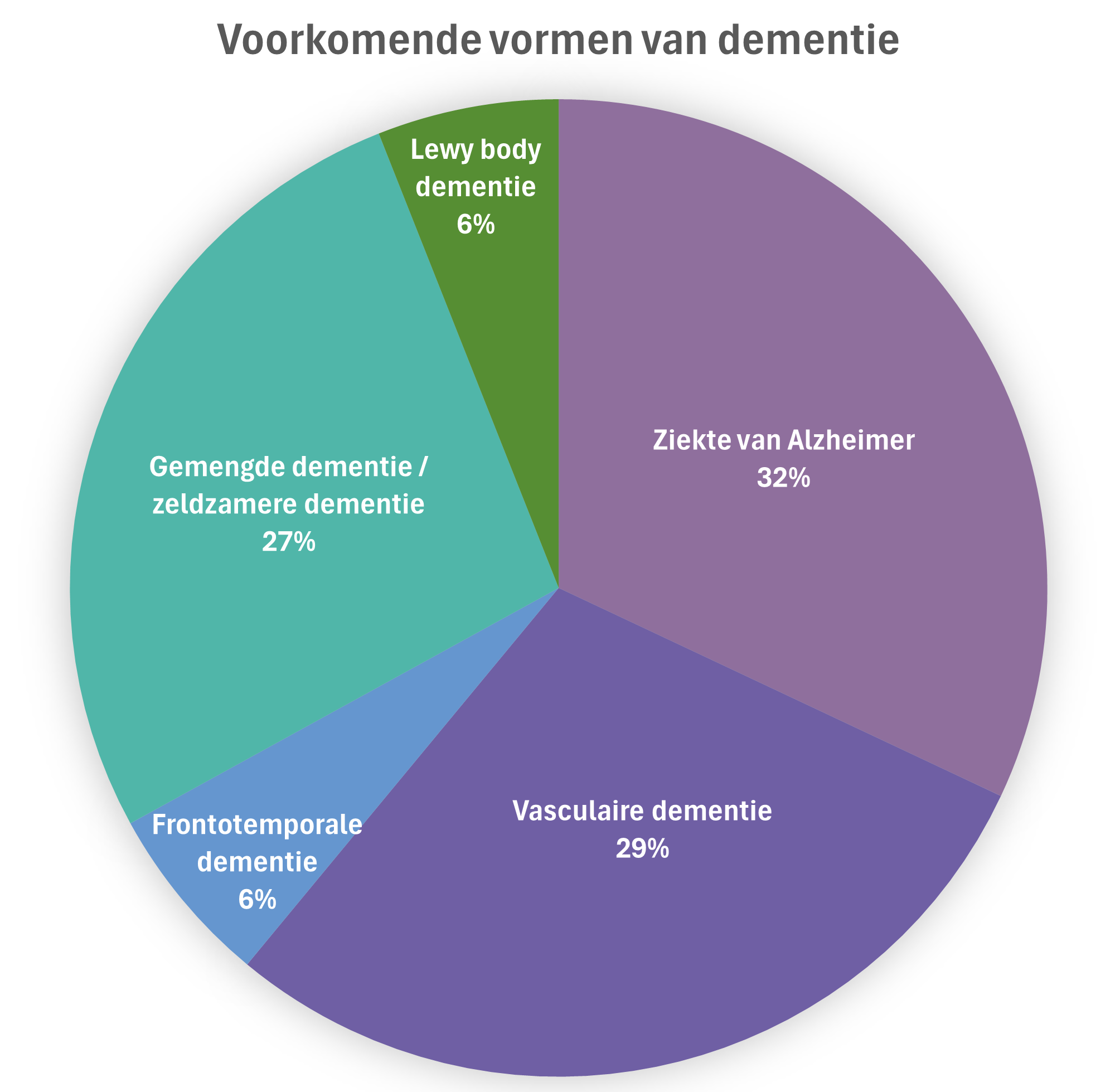
Er zijn verschillende soorten dementie, elk met zijn eigen kenmerken en onderliggende oorzaken. Enkele van de meest voorkomende types zijn:
-
Ziekte van Alzheimer:
Dit is de meest voorkomende oorzaak van dementie. Het wordt gekenmerkt door de ophoping van bèta-amyloïde plaques en tau-eiwit klusters in de hersenen, wat leidt tot verlies van zenuwcellen en hersenweefsel. -
Vasculaire dementie:
Dit type dementie treedt op wanneer er schade is aan de bloedvaten in de hersenen, vaak als gevolg van beroertes of andere aandoeningen die de bloedstroom naar de hersenen beïnvloeden. Symptomen kunnen zich bijvoorbeeld uiten als moeilijkheden met redeneren, beoordelen of problemen met het geheugen. -
Lewy body dementie:
Lewy body dementie wordt gekenmerkt door de aanwezigheid van abnormale eiwitophopingen genaamd Lewy bodies in de hersenen. Symptomen kunnen visuele hallucinaties, bewegingsstoornissen, schommelingen in alertheid en problemen met denken en redeneren omvatten. -
Frontotemporale dementie:
Dit type dementie wordt veroorzaakt door schade aan de frontale en temporale kwabben van de hersenen. Het beïnvloedt vaak gedrag, persoonlijkheid en taalvaardigheden, eerder dan geheugen. - Geschat wordt dat de overige 27% lijden aan meer dan één type dementie, bekend als gemengde dementie, of een zeldzamere vorm.
Invloed van genetica op het risico van de ziekte van Alzheimer
APOE gen
Het apolipoproteïne E (APOE) gen geeft instructies voor het maken van een eiwit genaamd apolipoproteïne E. Dit eiwit helpt het lichaam vetten, zoals cholesterol, te verwerken. De aanwezigheid van het APOE-gen, specifiek de APOE-ε4 versie, is de meest bekende genetische risicofactor voor late-onset Alzheimer. Elke persoon erft een combinatie van drie versies van het APOE-gen:
- ε2, de "beschermende" versie
- ε3, de "gezonde" versie en de meest voorkomende
- ε4, de "risicovolle" versie en de zeldzaamste
Het hebben van één kopie van het ε4-allel verhoogt het risico op het ontwikkelen van late-onset Alzheimer's ongeveer drie keer; personen die twee kopieën van het allel erven, lopen een nog groter risico, een geschat risico van acht tot twaalf keer. Dit betekent nog steeds niet dat je met twee ε4 allelen gegarandeerd Alzheimer zult krijgen. Aan de andere kant kan het hebben van de ε2-versie je risico verlagen in vergelijking met de ε3-versie. Van de ε3-versie wordt aangenomen dat het een neutraal effect heeft op het risico van Alzheimer.
In deze DNA-test identificeren we welke versies van het APOE-gen mensen hebben. Naast genetische mutaties in het APOE-gen worden ook andere genen geanalyseerd die, zij het in mindere mate, in verband zijn gebracht met een verhoogd of verlaagd risico op de ziekte van Alzheimer.
CLU gen
Het CLU-gen geeft instructies voor het maken van een eiwit genaamd Clusterin, dat betrokken is bij vele biologische activiteiten. Hoewel de precieze rol van Clusterin niet helemaal duidelijk is, lijkt het bij te dragen aan de celoverleving en het vermogen van het lichaam om weefsels te repareren.
In de context van de ziekte van Alzheimer suggereert onderzoek dat clusterin betrokken kan zijn bij de ontwikkeling of progressie van de ziekte. Individuen met bepaalde CLU-genvarianten kunnen enige bescherming hebben tegen de ziekte van Alzheimer. Sommige onderzoeken suggereren dat deze genetische variant kan leiden tot een betere bescherming van neuronen tegen de schadelijke effecten van amyloïde bèta-plaques en tau-tangles, wat het risico op de ziekte van Alzheimer kan verminderen.
CR1 gen
Het CR1-gen geeft instructies voor het produceren van een eiwit dat bekend staat als ComplementReceptor 1, dat een cruciale rol speelt bij het reguleren van het immuunsysteem.
Er is bewijs dat variaties in het CR1-gen kunnen bijdragen aan een hoger risico op het ontwikkelen van late-onset Alzheimer. Studies hebben bepaalde versies van een specifieke genetische marker, rs6656401, gekoppeld aan een verhoogde kans op het begin van de ziekte van Alzheimer. Hoewel de exacte mechanismen onduidelijk blijven, speculeren wetenschappers dat CR1 mogelijk invloed heeft op de verwijdering van beta-amyloïde, een eiwit dat de karakteristieke plaques vormt in de hersenen van Alzheimerpatiënten. Variaties in het CR1-gen zouden mogelijk van invloed kunnen zijn op hoe efficiënt het eiwit beta-amyloïde opruimt, wat potentieel kan leiden tot een grotere ophoping van plaques en daaropvolgende hersenschade.
PICALM gen
Het PICALM-gen bevat instructies voor het maken van een eiwit genaamd Phosphatidylinositol Binding Clathrin Assembly Protein, dat belangrijk is voor een proces genaamd clathrine-gemedieerde endocytose. Dit proces helpt cellen stoffen op te nemen uit hun omgeving.
PICALM is belangrijk geworden in het onderzoek naar de ziekte van Alzheimer omdat er een link met de aandoening is gevonden. Verschillende studies hebben gevonden dat variaties in het PICALM-gen tot de sterkste genetische risicofactoren voor de ziekte van Alzheimer behoren.






Volg ons op...